由悉尼科技大學(UTS)領銜的國際研究團隊,近日於《Nature Nanotechnology》發表關鍵性文章,揭示了一項名為「奈米粒子介導標靶嵌合體」(NPTACs)的開創性技術。該技術能有效消除體內有害致病蛋白,為過去難以攻克的「不可成藥」(undruggable)蛋白提供了全新的解決途徑,對失智症與腦癌等重大疾病的治療具有轉化性意義。
 |
| /news/2026/01/25/1006382960S.jpg |
這項研究由UTS奈米醫學首席教授史冰陽主導,並與哥倫比亞大學Kam Leong教授及河南大學鄭蒙教授共同合作。史教授指出,當體內蛋白質發生突變或錯誤折疊時,會干擾正常的細胞運作並引發疾病,而許多癌症與神經退化性疾病的致病蛋白,因其結構特殊,往往具備極強的抗藥性。
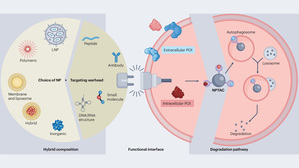
為了解決此難題,研究團隊開發出NPTACs奈米粒子,這是一種可客製化的微小粒子,能精準結合並降解特定的致病蛋白。這項技術不僅能處理細胞內的蛋白,也能鎖定細胞外的有害物質,將其引導至人體天然的「回收系統」中進行分解與移除,從根本上消除病灶。
標靶蛋白降解(TPD)目前是生物技術領域增長最快的賽道之一,吸引了包括Pfizer、Bayer與Roche在內的醫藥巨頭投入數十億美元資金。然而,傳統降解工具長期受限於組織穿透力不足及合成過程複雜等問題,尤其在面對實體腫瘤或腦部疾病時,難以突破生理屏障。
NPTACs策略則成功克服了這些瓶頸。其關鍵優勢包括:具備穿透血腦屏障的能力、具備「即插即用」的模組化特性能快速適應多種目標蛋白,以及採用FDA核可材料使具備臨床轉化的量產潛力。此外,該技術還能整合診斷與治療功能,實現多效合一的精準醫療。
目前NPTACs已在臨床前研究中展現強大成效,成功針對EGFR與PD-L1等關鍵腫瘤蛋白進行降解。隨著標靶蛋白降解市場預計在2030年突破100億美元規模,研究團隊正積極尋求全球戰略合作夥伴,加速臨床開發與監管審批流程,為次世代精準醫療奠定基礎。